近日,我院罗涛副研究员联合复旦大学高谦教授团队及国内外多家机构在Nature Communications在线发表了题为“Population genomics provides insights into the evolution and adaptation to humans of the waterborne pathogen Mycobacterium kansasii”的论文。我院罗涛副研究员为论文共同第一作者及共同通讯作者,四川大学为论文第一单位。
水源性病原菌感染一直是人类健康的一大威胁。人类社会多种疫病(如霍乱、痢疾、伤寒等)都与水污染有关。近年来,随着污染的严格控制及水厂消毒净化工艺的提升,由水污染引发的传染病发病率大幅降低。然而,一些天然分布于水源中的病原菌感染率呈上升趋势,非结核分枝杆菌(NTM)是其中之一。目前已知的NTM有190余种,其中仅少数可导致人类疾病,包括鸟分枝杆菌、脓肿分枝杆菌、堪萨斯分枝杆菌等,其中堪萨斯分枝杆菌因其致病性强、临床分离率高且可引发结核病样症状而广受关注。然而目前为止,堪萨斯分枝杆菌的传播途径、致病因子以及其宿主适应机制尚不明确。
本研究对从全球17个国家不同年代(1990-2015)收集的堪萨斯分枝杆菌进行了基因组测序和群体基因组学分析(图1)。结果表明,全球各地的堪萨斯分枝杆菌间有较近的亲缘关系,其祖先大致起源于上世纪初的欧洲,然后随全球化进程播散到世界各地。分析发现,大多数临床菌株基因组上都存在大量其他水源分枝杆菌的核酸片段,这与只能在人群中传播的结核分枝杆菌截然不同;该结果为堪萨斯分枝杆菌主要通过水源性途径感染人类这一前期推论提供了首个遗传学证据。进一步分析1990-1996年间澳大利亚发生的一次爆发流行证实,临床聚集性感染是由不同个体暴露于带菌水体所致,并未发现“人传人”证据。
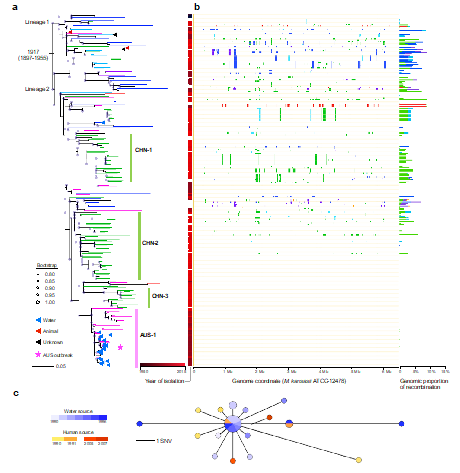
图1.堪萨斯分枝杆菌群体结构、同源重组及聚集性病例研究
通过比较基因组学分析,本文发现堪萨斯分枝杆菌保留了丙酸盐代谢相关基因簇(图2),使其在宿主体内分解胆固醇等营养物质过程中不会因丙酸盐堆积产生毒副作用。此外,研究还揭示了堪萨斯分枝杆菌特异性致病因子EspE样蛋白,该蛋白在堪萨斯分枝杆菌中发生了多次扩张,很可能通过分枝杆菌毒力相关分泌系统ESX-1分泌到细胞表面起到调控宿主免疫的作用。
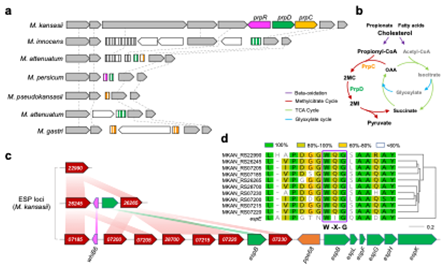
图2.堪萨斯分枝杆菌丙酸盐代谢基因及其特异性致病因子EspE样蛋白编码基因簇
通过生物信息学及表型分析,本文进一步揭示了堪萨斯分枝杆菌一系列的宿主适应机制(图3),包括:通过可遗传变异上调锌、铁等金属离子摄取相关基因以抵抗宿主金属离子饥饿;通过启动子突变上调脂质转运及乳酸代谢相关基因增强其利用宿主营养物质的能力;通过基因失活突变特异性丢失细菌细胞壁亲水性脂质LOS,从而增强其细胞壁疏水性以适应宿主体内环境同时调控宿主免疫的机制。
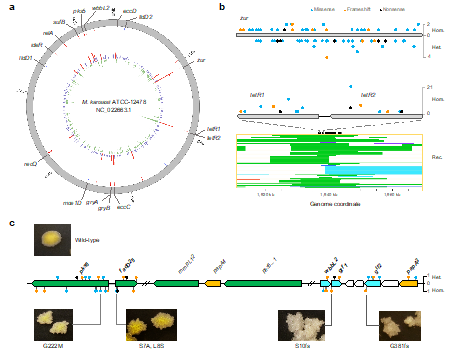
图3.堪萨斯分枝杆菌宿主适应机制
最后本文指出,虽然目前并未发现堪萨斯分枝杆菌“人传人”证据,但考虑其临床感染症状与结核病高度相似,以及其不断增强的宿主适应能力,公共卫生部门需加强对该病原体的监测,以防其进化为能在人群中传播的专性致病菌。
原文链接:https://www.nature.com/articles/s41467-021-22760-6